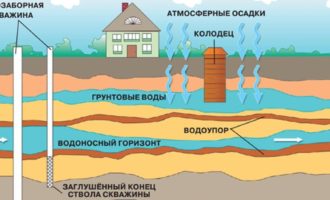
Жидкость занимает больший объем в организме человека. Выполнение физиологических функций в человеческом теле, зависит от степени загрязнения воды тяжелыми металлами. Для поддержания обменных процессов в организме, требуется не менее 2 литров жидкости в день. И, на первое место в потреблении питьевых ресурсов, выходит очистка воды от тяжелых металлов.
Компания «СИГНАЛ-ПАК» предлагает качесвенные дозаторы для пищевой промышленности https://www.signal-pack.com/oborudovanie/dozatory-dlya-pishevoy-promishlennosti/, у которых отсутствуют какие-либо вредные вещества в составе.
Определение содержания тяжелых металлов в воде
Понятие «тяжелый металл» относится к сфере охраны природы и здравоохранения. В эту группу относят полуметаллы и металлы, имеющие токсичные свойства и поражающую биологическую активность. Немало металлов входит в перечень необходимого микроэлементного уровня для нормального протекания биологических процессов и функционирования систем живого организма.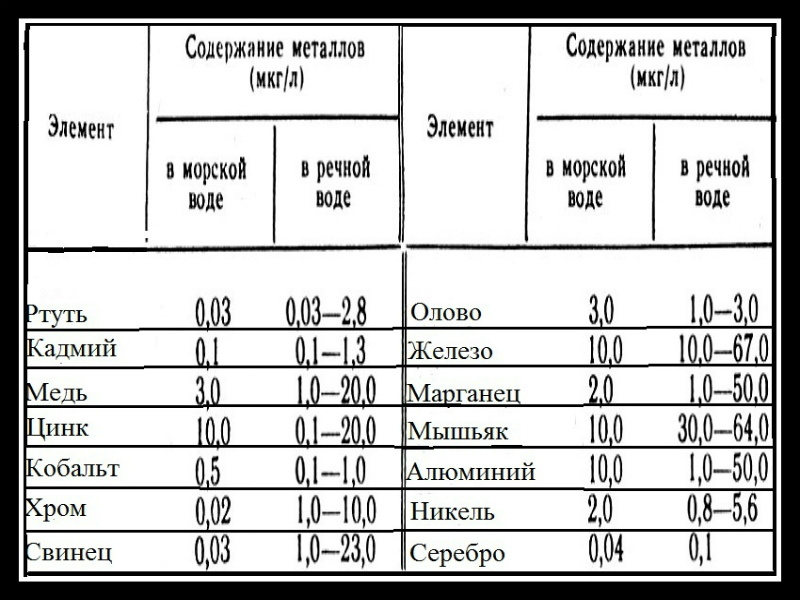
Токсичные химические элементы, попадая в организм человека с водой, имеют свойство аккумулироваться. Но, большую опасность представляет их способность к биомагнификации. Когда по пищевой цепочке: загрязненная вода – растения или почва – рыба или животное – человек, тяжелые металлы увеличивают свое вредоносное действие в сотни раз. Понимание, к чему приводит загрязнение воды тяжелыми металлами, подвигло человечество на внимательное отношение к природным ресурсам.
ГОСТ по питьевой воде на содержание тяжелых металлов
Таблица 1. ПДК тяжелых металлов в воде
| Показатели | СанПиН 2.1.4.1074-01 | ВОЗ | ЕС | |||
| Ед. изм. | ПДК | Показ. вред. | Класс опасн. | |||
| Алюминий (Al3+) | мг/л | 0,5 | с.-т | 2 | 0,2 | 0,2 |
| Барий (Ва2+) | мг/л | 0,1 | с.-т | 2 | 0,7 | 0,1 |
| Ванадий (V) | мг/л | 0,1 | с.-т | 3 | 0,1 | – |
| Железо (Fe, суммарно) | мг/л | 0,3(1,0) | орг. | 3 | 0,3 | 0,2 |
| Кадмий (Cd, суммарно) | мг/л | 0,001 | с.-т | 2 | 0,003 | 0,005 |
| Кобальт (Со) | мг/л | 0,1 | с.-т | 2 | – | – |
| Медь (Сu, суммарно) | мг/л | 1 | орг. | 3 | 2,0(1,0) | 2,0 |
| Мышьяк (As, суммарно) | мг/л | 0,05 | с.-т | 2 | 0,01 | 0,01 |
| Ртуть (Hg, суммарно) | мг/л | 0,0005 | с.-т | 1 | 0,001 | 0,001 |
| Свинец (Pb, суммарно) | мг/л | 0,03 | с.-т | 2 | 0,01 | 0,01 |
| Селен (Se, суммарно) | мг/л | 0,01 | с.-т | 2 | 0,01 | 0,01 |
| Серебро (Ag+) | мг/л | 0,05 | – | 2 | – | 0,1 |
| Хром (Cr3+) | мг/л | 0,5 | с.-т | 3 | – | – |
| Хром (Cr6+) | мг/л | 0,05 | с.-т | 3 | 0,05 | 0,05 |
| Цианиды (CN-) | мг/л | 0,035 | с.-т | 2 | 0,07 | 0,05 |
| Цинк (Zn2+) | мг/л | 5 | орг. | 3 | 3,0 | 5,0 |
Примечания:
с.-т – санитарно-токсикологический показатель;
орг. – органолептический показатель;
значения в скобках, могут приниматься в отдельных районах по указанию санитарного врача.
Как видно из таблицы, многие химические элементы находятся в виде различных лиганд, гидролизных или полимеризованных комплексов. Кроме прямого удаления загрязнений, немалое значение придается очистке воды от ионов тяжелых металлов и их соединений. Если присутствует значительное количество ионов тяжелых металлов в воде, увеличивается токсичность элемента из-за проявления кумулятивного эффекта.
Насыщенность токсичными химическими элементами питьевых ресурсов оценивается не только по их общему содержанию, но и по связанным и свободным формам, учитываются и соли тяжелых металлов в воде.
Распознавание нежелательных примесей сложной формы, проводят спектрометрическим или электрохимическим способом. Важное место в точном определении концентрации тяжелых металлов в воде занимает атомно-абсорбционная спектрометрия. Она подразделяется:
- на FAAS – плазменная атомизация;
- на GF AAS – электротермическая атомизация в графитовой ванночке.
Для выделения спектров нескольких металлов одновременно применяют эмиссионную или масс-спектрометрию, с плазмой связанной индукцией. Электрохимический способ распознавания основан на анализе вольт-амперных характеристик. Это сложные лабораторные методы определения уровня загрязнения воды тяжелыми металлами, на фото показаны:
- химическая лаборатория городской водозаборной станции;
- спектрометрический прибор для измерения тяжелых металлов в воде.


Методы очистки воды от тяжелых металлов
В зависимости от результатов проведенного анализа воды на тяжелые металлы, выбирается метод очистки, иногда их приходится комбинировать. Это может быть:
- использование сорбентов для поглощения
- перевод в нерастворимые соединения через ионный обмен;
- мембранный фильтр воды для тяжелых металлов;
- гальваническая очистка;
- применение магнитного поля;
- дистилляция с последующим конденсированием.
Абсорбенты и мембранные фильтры, самые простые и недорогие способы очистки, и нашли широкое применение в бытовых очистных устройствах. Выпаривание, слишком энергозатратный метод и редко применяется, несмотря на высокий уровень очищения жидкости.
Ионно-обменный метод очистки дает высокие результаты по удалению примесей. Технология реализуется с помощью ионообменных смол, собирающих на своей поверхности ионы тяжелых металлов. Регенерацию смолы проводят кислотой. Металлы в ионной форме могут осаждаться с помощью изменения pH до значения 9,0÷10,5. И затем, отделяют осадок от жидкости.
При высоком насыщении жидкости ионами меди, хорошие результаты дает гальванический процесс. В загрязненную воду опускают электроды с пористой структурой и большой активной поверхностью. При подаче электричества, ионы меди восстанавливают атомарное состояние и осаждаются на электроде.
На водоочистных станциях, куда попадают и городские и производственные стоки, применяют цикличные процессы обработки воды, куда последовательно включают несколько операций.